Crédits photo: ScenTree SAS
| Entreprise | Nom de l'ingrédient | ID | Commentaires | Naturalité | Certifications | Pureté | Nom latin | Partie traitée | Origine géographique | MOQ |
|---|---|---|---|---|---|---|---|---|---|---|
|
|
Sandela® - 30gr | - |
Visit website
|
- | - | - | - | - | - |
Général
-
N° CAS : 3407-42-9
-
N° EINECS : 222-294-1
-
N° FEMA : Donnée indisponible.
-
N° FLAVIS : Donnée indisponible.
-
N° JECFA : Donnée indisponible.
-
Aspect : Liquide visqueux incolore
-
Densité : 0,972
-
Tenue : Fond
-
Gamme de prix : €€
Propriétés physico-chimiques
-
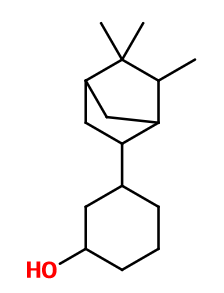
Formule brute : C16H28O
-
Masse molaire : 236,4 g/mol
-
Log P : 5,27
-
Point de fusion : Donnée indisponible.
-
Point d'ébullition : 160°C (à4 hPa)
-
Seuil de détection : Donnée indisponible.
-
Optical rotation : Donnée indisponible
-
Pression vapeur : Donnée indisponible
-
Indice de réfraction @20°C : Donnée indisponible
-
Valeur d'acide : Donnée indisponible.
-
Point éclair : 152°C
Utilisations
Utilisations :
Le Sandela® est utilisé dans des notes boisées et des reproductions de santal. A combiner avec le Sandalore® pour plus de facettes. Est souvent solubilisé à 85% dans le Myristate d'isopropyle, avant dilution dans l'alcool.
Découverte :
1942
Présence dans la nature :
Le Sandela® n'est pas disponible à l'état naturel.
Isoméries :
Le Sandela® est le seul des isomères issus de la synthèse décrite ci dessus à être odorant et à présenter un réel intérêt pour la parfumerie. L'Ambroxan®, le Cedramber® et la Muscénone® sont des isomères de constitution du Sandela®. Leur odeur peut aussi être boisée, ou encore musquée. Elle reste très différente quoi qu'il en soit.
Précurseurs de synthèse :
La Sandela® n'est pas précurseur de la synthèse d'un autre composé d'intérêt olfactif.
Voies de synthèse :
Le Sandela® fait partie d'un mélange d'isomères synthétisé par réaction entre le Camphène et le Guaiacol, en présence d'un acide de Lewis comme le trifluorure de bore. Durant cette première étape, le Camphène subit un réarrangement sous trois formes : Isocamphyl, Isofenchyl et Isobornyl. Cela crée le mélange d'isomères. Une hydrogénation catalytique sous haute température de ces dérivés permet d'obtenir un nouveau mélange de plus d'isomères encore. En effet, la moitié terpénique de la molécule finale peut être en position axiale ou équatoriale par rapport à l'autre moitié de la molécule. Le 3-trans-Isocamphylcyclohexanol, correspondant au Sandela®, fait partie des isomères du mélange. Il en est isolé par distillation fractionnée. Un autre procédé de synthèse part du Cathécol plutot que du Guaiacol, et permet d'obtenir une plus grande proportion de Sandela® dans le mélange final (surtout si l'étape d'hydrogénation est faite sous haute pression et catalysée au cobalt).
Réglementation & IFRA
Allergènes :
Cet ingrédient ne contient pas d'allergènes.
51ème amendement :
Cet ingrédient n'est pas réglementé par le 51ème amendement


