Crédits photo: ScenTree SAS
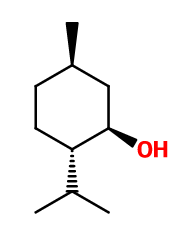
L-Menthol
(1R,2S,5R)-5-methyl-2-propan-2-ylcyclohexan-1-ol ; L-hexahydrothymol ; Levomenthol ; L-menthacamphor ; Trans-para-menthan-cis-ol ; (1R,2S,5R)-5-methyl-2-(propan-2-yl)cyclohexanol ; L-peppermint camphor ; 1-isopropyl-4-methyl cyclohexan-2-ol

Crédits photo: ScenTree SAS
| Entreprise | Nom de l'ingrédient | ID | Commentaires | Naturalité | Certifications | Pureté | Nom latin | Partie traitée | Origine géographique | MOQ |
|---|---|---|---|---|---|---|---|---|---|---|
|
|
Menthol - 30 Gr | - |
Visit website
|
- | - | - | - | - | - | |
|
|
MENTHONE L-23 | M_0050650 |
Visit website
|
Naturel | - | - | - | - | - | |
|
|
L-Menthol FCC | 30564715 |
Visit website
|
Molecule | - | - | - | - | - | |
|
|
L-Menthol FCC BMBcert™ | 30775033 |
Visit website
|
Molecule | - | - | - | - | - | |
|
|
L-Menthol Flakes FCC | 30564716 |
Visit website
|
Molecule | - | - | - | - | - | |
|
|
L-Menthol Flakes FCC BMBcert™ | 30775034 |
Visit website
|
Molecule | - | - | - | - | - |
Général
-
N° CAS : 2216-51-5
-
N° EINECS : 218-690-9
-
N° FEMA : 2665
-
N° FLAVIS : Donnée indisponible.
-
N° JECFA : Donnée indisponible.
-
Aspect : Solide blanc
-
Densité : 0,89
-
Tenue : Tête
-
Gamme de prix : €€
Propriétés physico-chimiques
-
Formule brute : C10H20O
-
Masse molaire : 156,27 g/mol
-
Log P : 3,15
-
Point de fusion : 42°C
-
Point d'ébullition : 219°C
-
Seuil de détection : Donnée indisponible.
-
Optical rotation : Donnée indisponible
-
Pression vapeur : Donnée indisponible
-
Indice de réfraction @20°C : Donnée indisponible
-
Valeur d'acide : Donnée indisponible.
-
Point éclair : 94°C
Utilisations
Utilisations :
Le L-Menthol est utilisé dans les reconstitutions de menthe, dans les parfums masculins, pour un apport d'envolée et pour booster la tête.
Découverte :
1907
Présence dans la nature :
Le L-Menthol est majoritairement produit à l'état naturel, à partir de la Mentha arvensis HE, à plus de 15 000 tonnes par an. L'huile essentielle, contenant jusqu'à 80% de Menthol, peut être glaçée pour faire cristalliser le L-Menthol, séparé de l'huile par centrifugation. Une recristallisation est alors nécessaire si l'on veut obtenir une plus grande pureté. L'huile essentielle contenant alors 30 à 50% de Menthone® peut être à nouveau mobilisée pour produire du Menthol hémisynthétique. Une hydrogénation catalytique de l'huile forme du L-Menthol et du Néomenthol-D. Les esters de menthyle présents sont saponifiés et une nouvelle cristallisation du Menthol peut avoir lieu. La Menthe piperita HE peut aussi servir pour extraire le L-Menthol naturel.
Isoméries :
Le Menthol possède quatre couples d'isomères (lévogyre et dextrogyre), dérivant de la présence de trois carbones asymétriques dans la molécule. Le Menthol, le Néomenthol, l'Isomenthol et l'Isonéomenthol font partie du mélange d'isomères. Seul le L-Menthol provoque une sensation de froid à l'olfaction. C'est d'ailleurs lui qui est le plus utilisé en parfumerie. Le Citronellol, le Dihydromyrcénol et la Patchone® font partie des isomères de constitution du Menthol. Ceux-ci ont des odeurs bien différentes du Menthol, tant elles sont plus florales ou terreuse et boisée.
Précurseurs de synthèse :
Le L-Menthol est précurseur, comme ses isomères, de la synthèse de plusieurs composés d'intérêt olfactif. Une hydrogénation catalytique de la molécule amène à la formation de para-Menthane. Une oxyation par l'acide chromique ou une déshydrogénation conduit à la synthèse de Menthone®. Une déshydrogénation sans catalyseur conduit à la formation de 3-para-Menthène. Enfin, une estérification avec des acides carboxyliques et en présence d'un catalyseur acide synthétise des esters de menthyl. L'estérification avec l'acide benzoïque est utilisé à échelle industrielle pour la résolution d'un Menthol racémique.
Voies de synthèse :
Le L-Menthol en lui-même peut être synthétisé de plusieurs manières. La première est le résultat d'une cyclisation du Citronellal dextrogyre (obtenu par voie naturelle ou à partir du Myrcène), par réaction avec un acide de Lewis comme le chlorure de zinc. Le produit obtenu par cette cyclisation est un mélange des isomères de l'Isopulegol (l'isomère lévogyre étant obtenu en majorité). Alors, les isomères de l'Isopulégol peuvent être séparés pour récupérer le constituant lévogyre et synthétiser le L-Menthol par hydrogénation catalytique. Cette hydrogénation peut aussi avoir lieu avant la séparation des Menthol (qui requiert alors un passage par une estérification des Menthol du mélange obtenu). Une deuxième voie de synthèse part de la Pipéritone lévogyre, pouvant être hydrogénée en présence du catalyseur au nickel de Raney. Un mélange des isomères du Menthol est obtenu, capables d'être séparés par saponification et cristallisation, en passant par une réaction d'estérification des Menthol. Un troisième procédé part du Delta-3-carène dextrogyre présent dans la Térébenthine HE. Une isomérisation en 2-Carène dextrogyre, suivie d'une pyrolyse en trans-2,8-p-Menthadiène. Une isomérisation de ce dernier synthétise l'Isoterpinolène dextrogyre. Une hydrogénation catalytique donne du 3-para-Menthène dextrogyre. Une dernière étape d'époxydation, suivie d'un réarrangement et d'une hydrogénation catalytique du composé obtenu permettent de former un mélange de Menthol, séparables par distillation fractionnée. Il existe un dernier procédé assez complexe partant du Thymol. Ce procédé n'est pas détaillé ici car nous manquons de source.
Réglementation & IFRA
Allergènes :
Cet ingrédient ne contient pas d'allergènes.
51ème amendement :
Cet ingrédient n'est pas réglementé par le 51ème amendement


